生産拠点
日本国内の工場で製造を行っております。
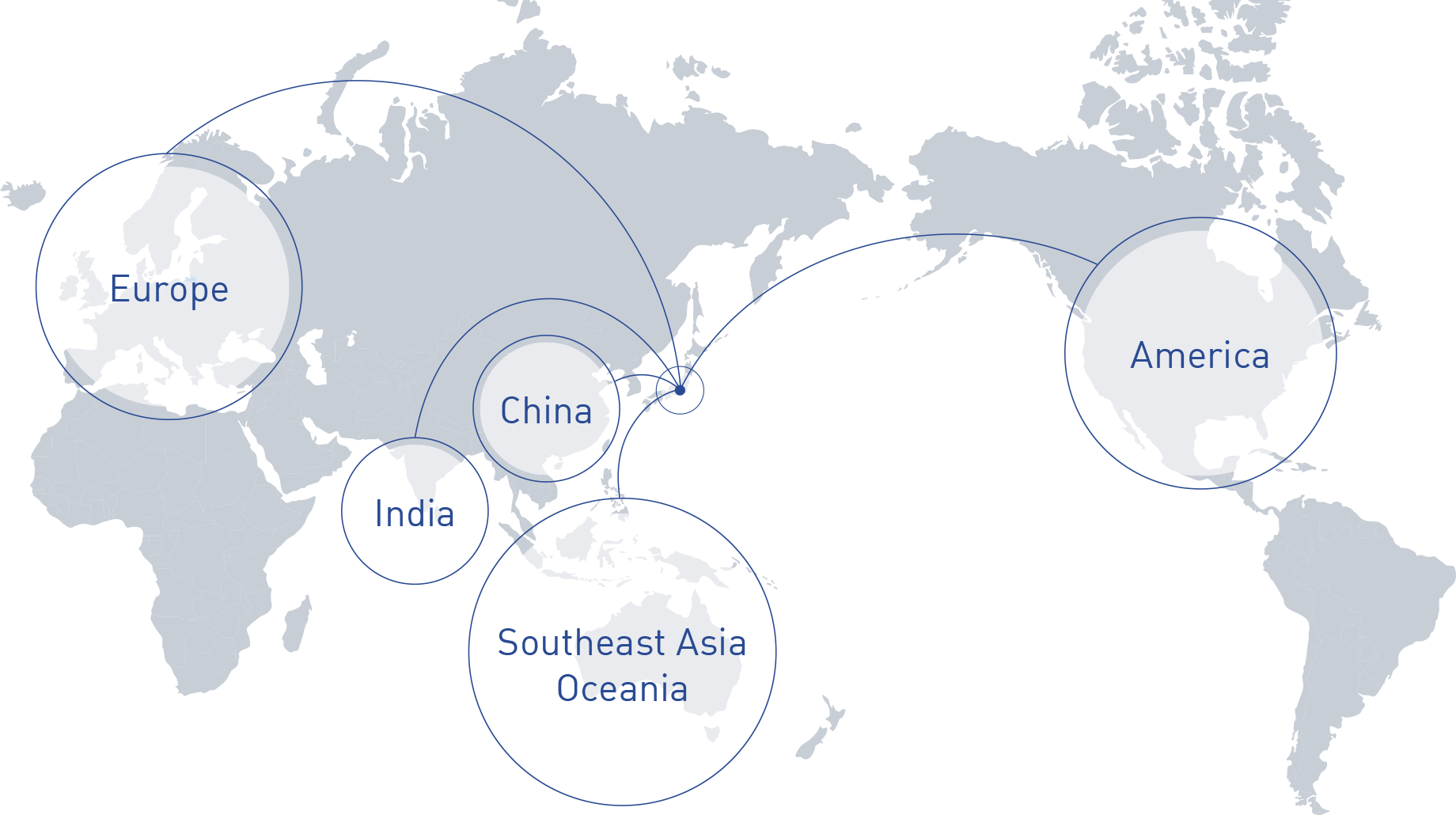
国内のみならず、グローバルに製品供給網を築いています。
日本国内生産工場
 大阪工場
大阪工場
- GMP管理
- ・GMP管理の医薬品製造
- ・医薬品製造業許可取得
主な生産品目
- ・医薬品製造用原料
- ・ライフサイエンス試薬 (PCR検出試薬・DNA抽出キット等)
- ・ケミカル試薬 (粉体・液体試薬)
- ・プロセス溶液
- ・臨床検査薬
査察・監査履歴
〈国内当局〉
- ・ 2017年10月 兵庫県薬務課によるGMP適合性調査 (定期・輸出)
- ・ 2018年10月 兵庫県薬務課によるGMP適合性調査 (一変)
- ・ 2021年10月 兵庫県薬務課によるGMP適合性調査 (定期・輸出)
- ・ 2025年10月 兵庫県薬務課によるGMP適合性調査 (定期・輸出)
〈国内および海外取引先の監査〉
実地の品質監査を毎年5~10件対応

| 所在地 | 兵庫県尼崎市 | 操業開始 | 1940年 |
|---|---|---|---|
| 敷地面積 | 23,332m2 | 認証 | ISO9001 ISO/IEC17025 ISO14001 ISO17034 |
| 事業所人員 | 約220名 |
 富士フイルムワコーケミカル株式会社広野工場
富士フイルムワコーケミカル株式会社広野工場
- GMP管理
-
・cGMP対応の原薬製造
・超低温釜、水素添加釜、耐フッ素釜、各粉砕機を保有
・医薬品製造業許可
主な生産品目
-
・医薬品 原薬・中間体
・高薬理活性 原薬・中間体
・治験薬 原薬・中間体
・ディスプレイ材料用薬品
・感光材料用薬品

| 所在地 | 福島県広野町 | 操業開始 | 1990年 |
|---|---|---|---|
| 敷地面積 | 139,000m2 | 認証 | ISO9001 ISO14001 |
| 事業所人員 | 約150人 |
 東京工場
東京工場
-
・ISO9001管理の医薬中間体製造
・研究所を併設
・試薬や少量多品種の化成品の生産
主な生産品目
-
・分析用試薬(認証標準物質、医薬品試験用試薬 等)
・各種溶媒(核酸合成用溶媒、HPLC用溶媒 等)
・重合開始剤
・半導体関連材料
・化粧品原料

| 所在地 | 埼玉県川越市 | 操業開始 | 1964年 |
|---|---|---|---|
| 敷地面積 | 約65,942m2 | 認証 | ISO9001 ISO/IEC17025 ISO14001 |
| 事業所人員 | 約350人 |
 富士フイルムワコーケミカル株式会社平塚工場
富士フイルムワコーケミカル株式会社平塚工場
-
・ISO管理の医薬品中間体製造
・キロラボ設備等マルチパーパス設備
主な生産品目
-
・医薬品中間体
・感光材料用薬品
・ディスプレイ材料用薬品
・X線診断用材料
・色材酸化防止剤
・インクジェット用色素

| 所在地 | 神奈川県平塚市 | 操業開始 | 1961年 |
|---|---|---|---|
| 敷地面積 | 36,000m2 | 認証 | ISO9001 ISO14001 |
| 事業所人員 | 約300人 |
 愛知工場
愛知工場
- GMP対応
- 培地製造
-
・大規模生産に適した医薬品中間体の製造
・高度な汚染防止管理
・GMP対応の粉体・液体培地製造
主な生産品目
-
・医薬品原料/中間体
・再生医療用培地「WakoVAC シリーズ 」
・WFI Quality Water
・プロセス溶液
・半導体関連材料

| 所在地 | 愛知県豊橋市 | 操業開始 | 2004年 |
|---|---|---|---|
| 敷地面積 | 176,000m2 | 認証 | ISO9001 ISO14001 |
| 事業所人員 | 約150人 |
 播磨工場
播磨工場
-
・一般化製品の中規模生産工場
・発酵技術を使用している唯一の生産工場
主な生産品目
-
・医薬品・化粧品原料
・アゾ重合開始剤
・機能性材料
・抗生剤、発酵試薬

| 所在地 | 兵庫県赤穂市 | 操業開始 | 1968年 |
|---|---|---|---|
| 敷地面積 | 21,132m2 | 認証 | ISO9001 ISO14001 |
| 事業所人員 | 約50人 |
 富士フイルムワコーケミカル株式会社宮崎工場
富士フイルムワコーケミカル株式会社宮崎工場
- GMP管理
-
・小スケールの原薬・中間体製造
・医薬品製造業許可取得
主な生産品目
-
・医薬品原料/中間体
・培地添加剤
・分析・研究用試薬
・臨床検査薬原料
・半導体関連材料

| 所在地 | 宮崎県宮崎市 | 操業開始 | 1986年 |
|---|---|---|---|
| 敷地面積 | 35,000m2 | 認証 | ISO9001 ISO14001 |
| 事業所人員 | 約70人 |
海外への供給
日本で生産された商品を各地のお客様にご使用いただいております。